

INTRODUCTION
•
✦
研究介绍
✦
•
研究背景
Background
小细胞肺癌(SCLC)约占肺癌病例的15%并且预后不良,大约2/3的患者处于广泛期(ES)疾病状态,5年总存活率只有1-5%。免疫检查点抑制剂结合以铂为主的化疗方案已经报道和延长的中位生存期有关。贝莫苏拜单抗是一种人源的抗PD-L1抗体,已经展现出和其他免疫检查点抑制剂相似的临床前抗肿瘤活性。安罗替尼与免疫检查点抑制剂有潜在的协同作用。有一项1b期剂量递增试验探究了安罗替尼和贝莫苏拜单抗结合展现了良好的安全性,并且6个ES-SCLC患者中有4个得到部分反应。
研究目的
Aim
探究化疗方案中加入贝莫苏拜单抗和安罗替尼是否能够在ES-SCLC的一线治疗展现协同效应以及化疗方案中只加入安罗替尼是否临床有益。
METHODS
•
✦
研究方法
✦
•
1 | ETER701 (NCT04234607) 是在中国72个地点进行的多中心双盲双模拟随机化安慰剂对照三期临床试验。所有有资格的病人被中央随机分配以1:1:1的比例接受以下三个治疗方案之一:1. 贝莫苏拜单抗+安罗替尼+依托泊苷/卡铂(EC),随后贝莫苏拜单抗和安罗替尼维持治疗;2. 贝莫苏拜单抗安慰剂+安罗替尼+EC,随后安罗替尼维持治疗;3. 贝莫苏拜单抗安慰剂+安罗替尼安慰剂+EC,随后安慰剂维持治疗。随机化方法是中央分层随机化。治疗分配屏蔽患者、他们的家人或者监护人、研究者、本地和中央放射学审查员,研究统计学家、参与数据清理和数据分析的数据管理人员、研究赞助人直到最终的数据库被锁定。中期分析是由独立的数据监察委员会以非盲方式进行的。 |
2 | ETER701试验评估两个主要有效性终点:无进展生存期(PFS)和总生存期(OS)。独立评审委员会 (IRC)根据RECIST 1.1评估PFS,定义为从随机化到第一次记录疾病或死亡的时间。OS定义为从随机化到死亡的时间。次要终点包括IRC根据RECIST1.1评估的客观应答率,定义为实现完全应答和部分应答的参与者比例。生存分析用Kaplan–Meier方法,用分层log-rank检验。风险比(HR)和相关95%置信区间(95%CIs)用分层Cox比例风险模型评估。治疗组之间应答率的差异用Cochran–Mantel–Haenszel检验评估。 |
3 | EQ-VAS问卷评估健康相关生活质量(HRQoL)。混合模型重复测量方法用来比较EQ-VAS从基线的变化。 |
FINDINGS
•
✦
研究发现
✦
•
1. 病人和治疗
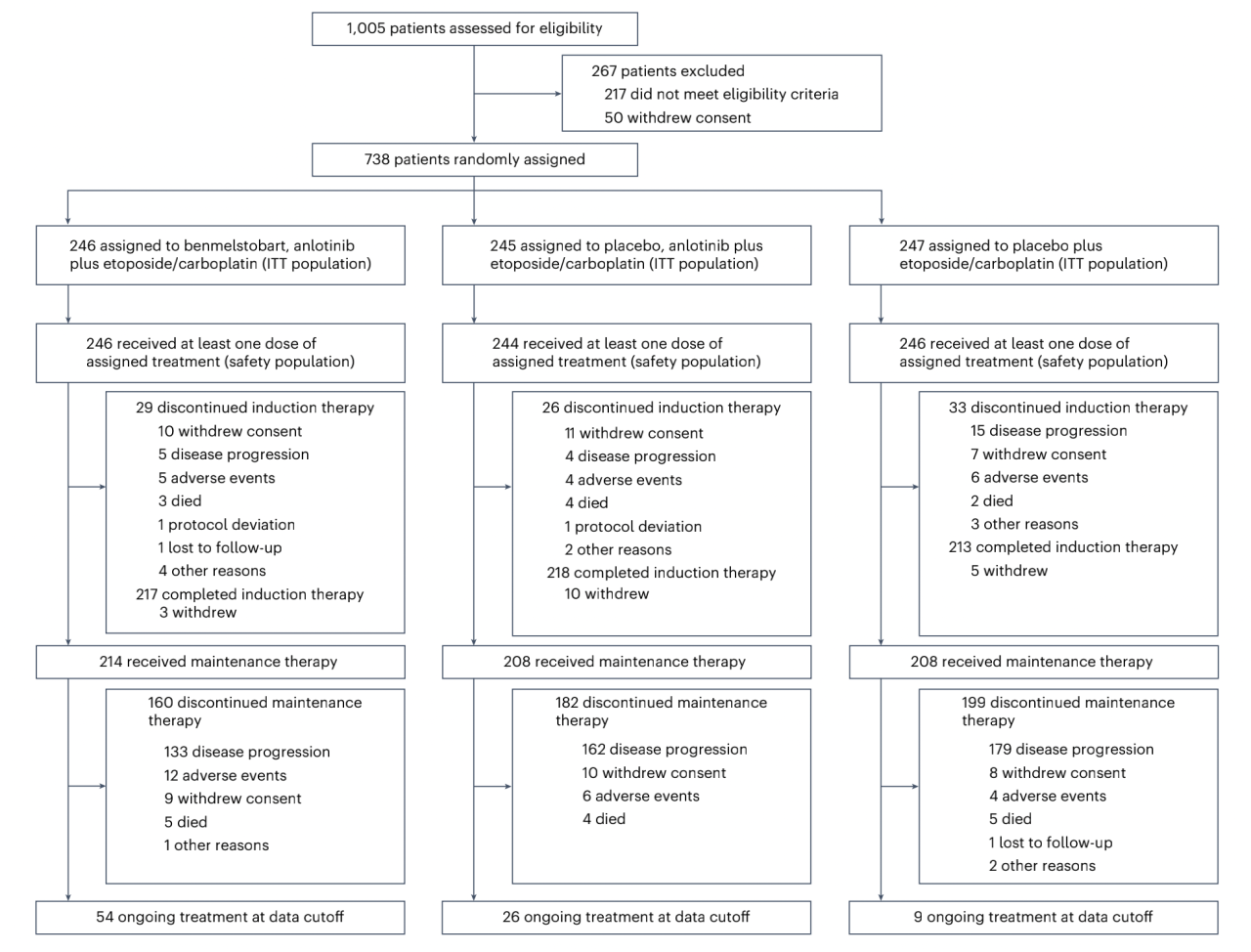
图1 患者处置
1005个病人进行了资格评估。738个病人随机接受治疗(意向治疗人群)。246个病人被分配接受贝莫苏拜单抗+安罗替尼+依托泊苷/卡铂(EC),245个接受安罗替尼+EC,247个接受EC(图1)。在738个患者中736人接受至少一剂方案治疗(安全人群)。在完成诱导治疗后,三组中214、208、208个患者分别接受计划的维持治疗。计划的总生存期中期分析中有89个病人仍处于指定的治疗中(图1)。
2. 主要终点
OS
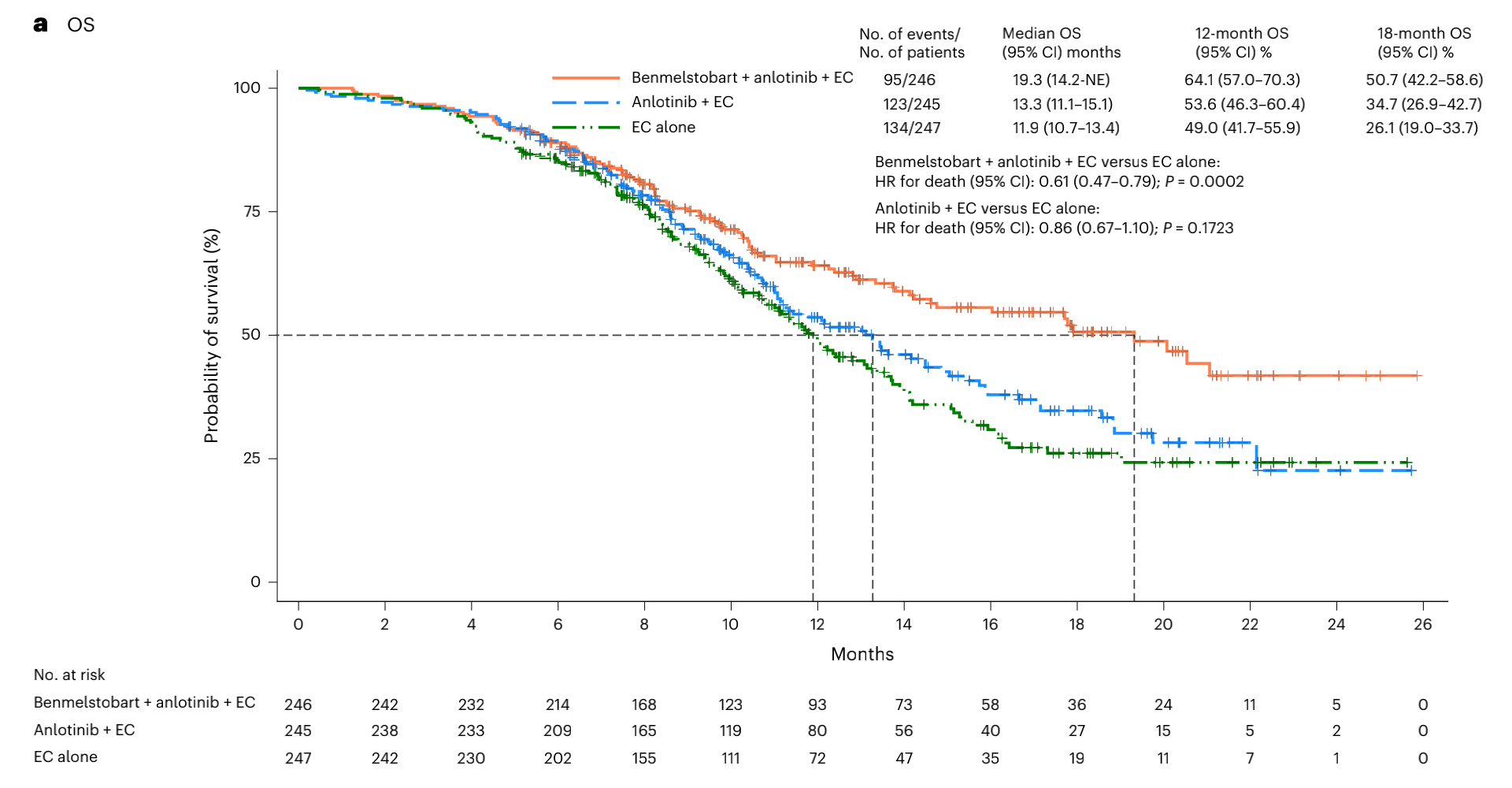
图2 意向治疗人群的OS
在预先指定的OS中期分析中,贝莫苏拜单抗+安罗替尼+EC组病人的中位OS大于EC组(19.3个月(95%CI 14.2-不可估计)vs 11.9个月(95%CI 10.7-13.4);P=0.0002;风险比0.61(95%CI 0.47-0.79)),满足统计学显著性预先指定的标准(图2)。安罗替尼+EC组的OS和EC组的没有显著差异(13.3个月(95%CI 11.1-15.1)vs 11.9个月(95%CI 10.9-13.4);风险比0.86(95%CI 0.67-1.10; P=0.1723))(图2)。
PFS
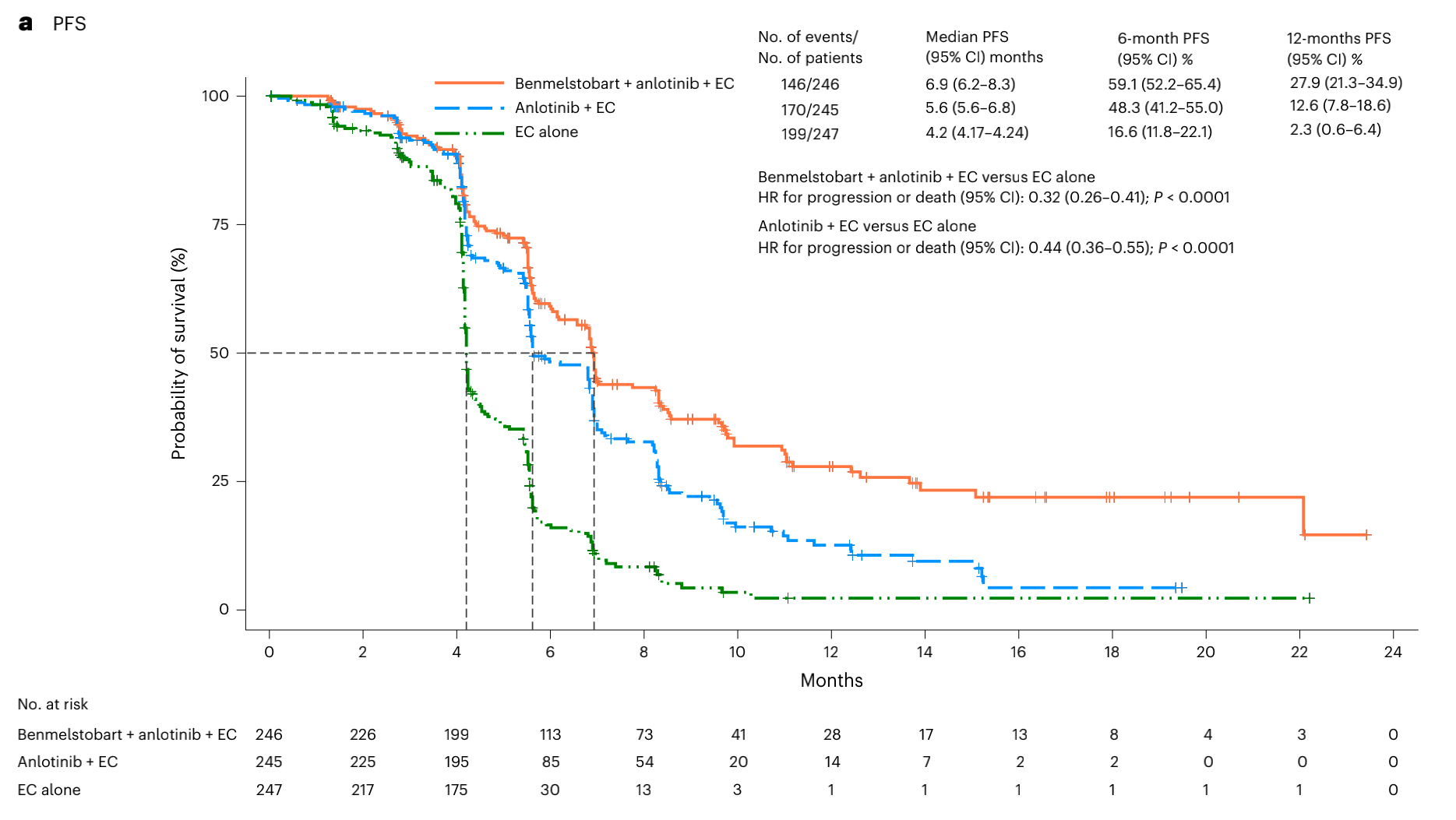
图3 意向治疗人群的PFS
PFS是由独立评审委员会(IRC)根据 RECIST 1.1评估的。在PFS的预先指定的最终分析中,贝莫苏拜单抗+安罗替尼+EC组的PFS显著比EC组的长(6.9 个月(95% CI 6.2–8.3)vs 4.2 个月(95% CI 4.17–4.24); 风险比0.32(95% CI 0.26–0.41);P < 0.0001)(图3)。安罗替尼+EC组的PFS显著比EC组的长(5.6 个月(95% CI 5.6–6.8)vs 4.2个月(95% CI 4.17–4.24);风险比0.44(95% CI 0.36–0.55);P < 0.0001)(图3)。
3.次要终点

表1 盲态独立中心评估根据RECIST1.1评价肿瘤反应
IRC评估的有客观应答的病人在贝莫苏拜单抗 + 安罗替尼+EC组占比是81.3%(95% CI 75.9–86.0;P=0.0001),安罗替尼+EC组中占比81.2%(95% CI 75.8–85.9;P=0.0003),两者都显著比EC组中占比高(66.8%; 95% CI 60.6–72.6)。有3个病人在贝莫苏拜单抗 + 安罗替尼 +EC组(1.2%),1个在安罗替尼+EC组(0.4%)得到完全应答(表1)。
4. 安全性
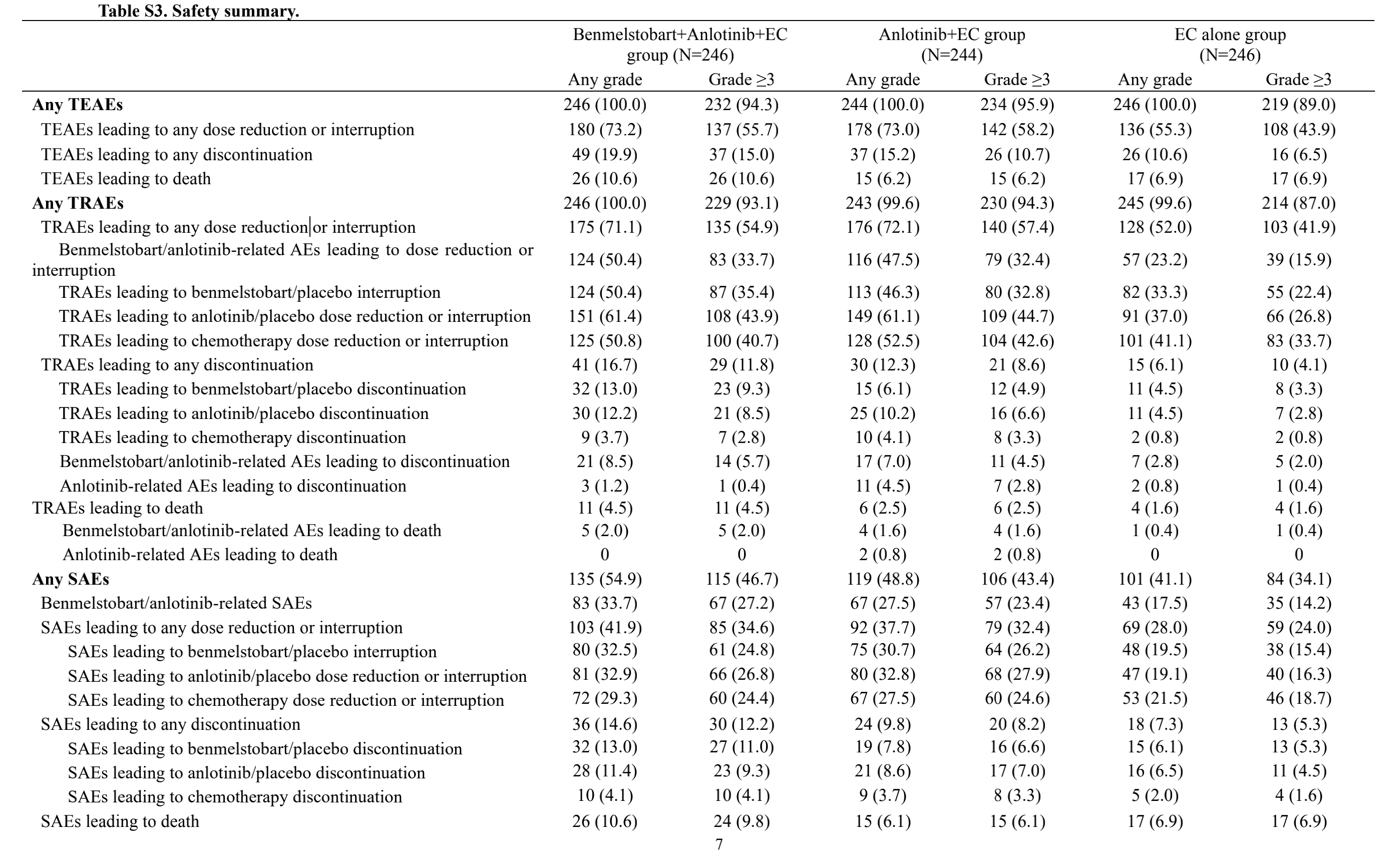
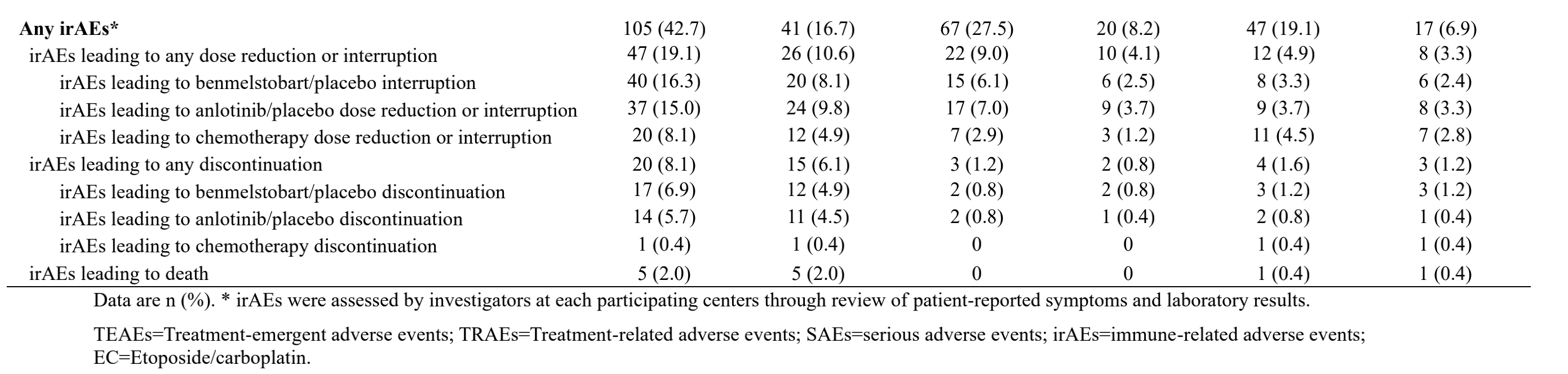
表2a 安全性总结
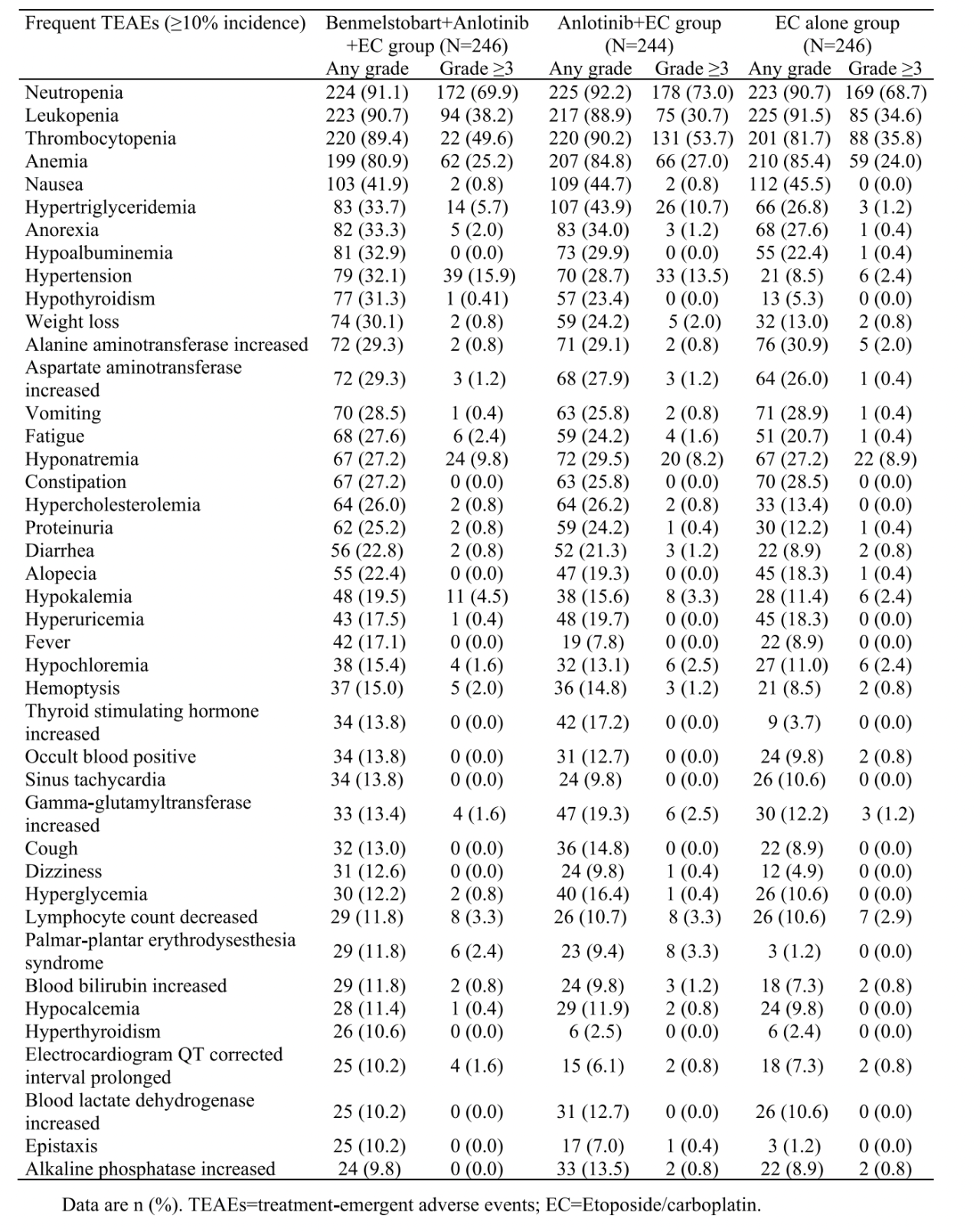
表2b 治疗期间出现的不良反应
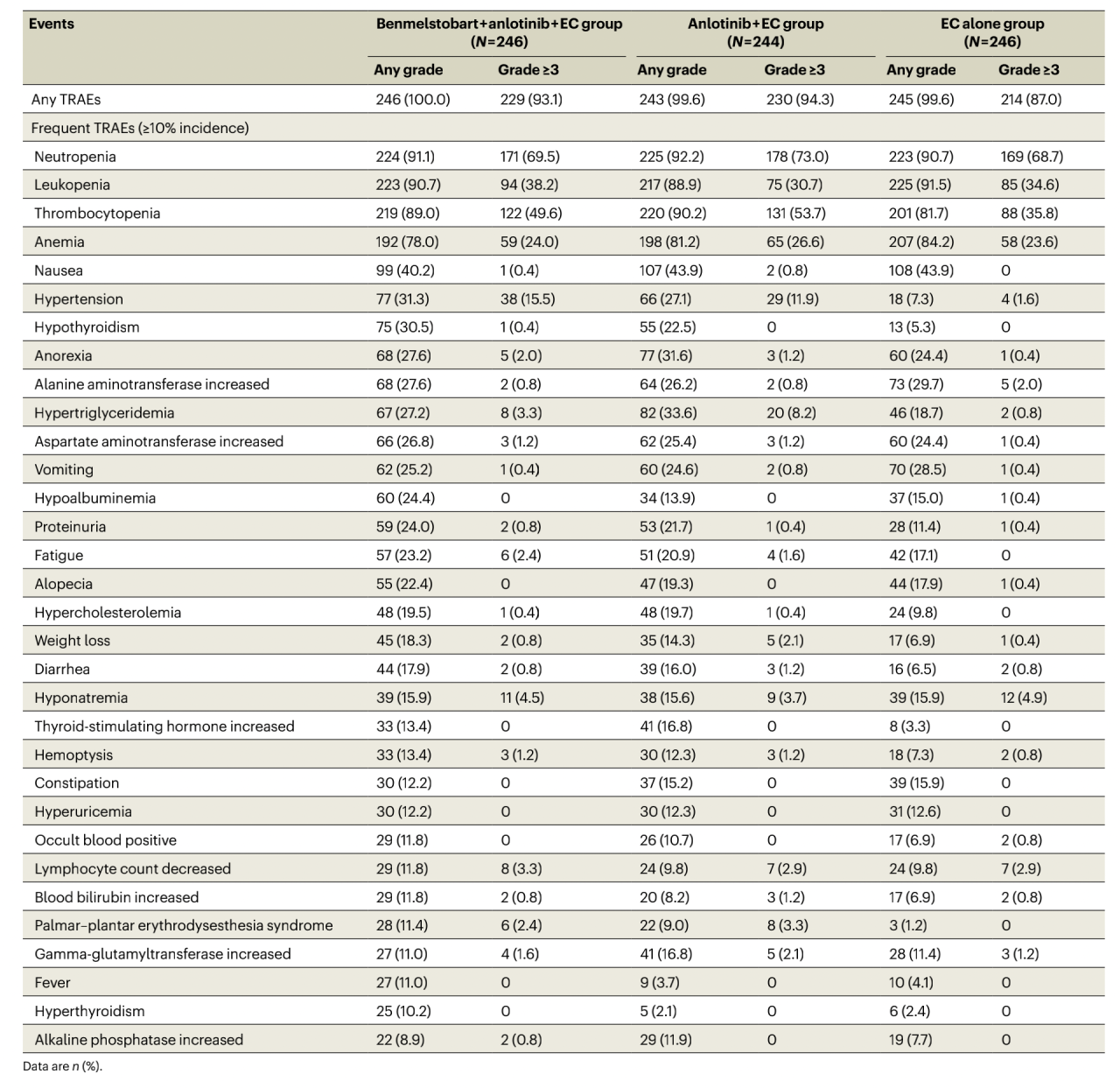
表2c 治疗相关不良反应
任何级别的治疗期间出现的不良事件100%发生在每个组中,在贝莫苏拜单抗 + 安罗替尼 +EC,安罗替尼 +EC,EC组中级别大于等于3的治疗期间出现的不良事件分别占94.3%,95.9%和89.0%(表2a),最常见的毒性包括血小板减少症,中性粒细胞减少症和白细胞减少症(表2b)。治疗相关不良反应在三组中的占比分别为100%,99.6%和99.6%,级别大于等于3的分别是93.1%, 94.3%和87.0%(表2c)。治疗相关不良反应导致死亡在三组中的比例分别为4.5%, 2.5%和1.6%(表2a)。严重不良事件在三组中的占比分别为54.9%, 48.8%和41.1%,级别大于等于3的分别是46.7%, 43.4%和34.1%(表2a)。免疫相关不良事件在三组中的占比分别为42.7%,27.5%,19.1,级别大于等于3的分别是16.7%, 8.2%和6.9%(表2a)。
5. 健康相关生活质量(HRQoL)
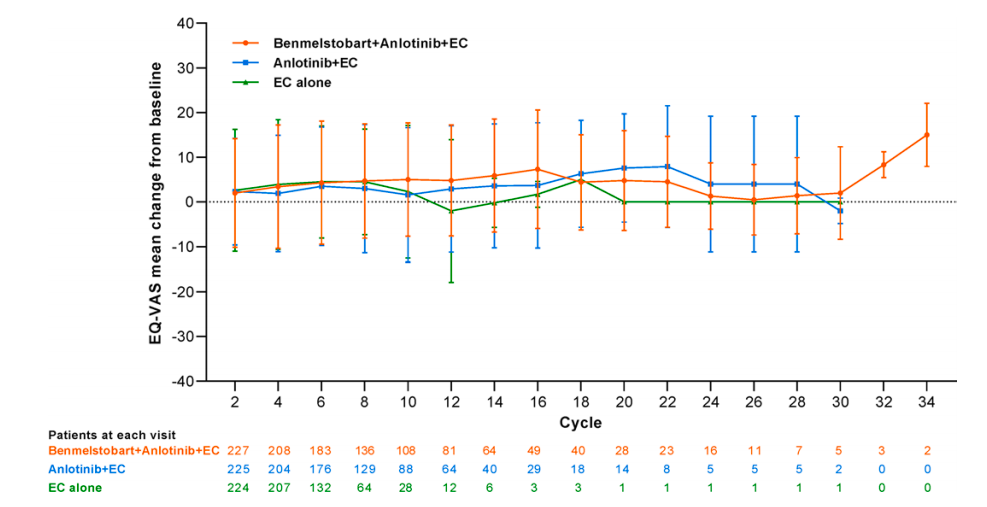
图4 患者报告的与健康相关的生活质量的结果
在所有意向治疗人群治疗组中,EuroQol visual analog scale (EQ-VAS)分数从基线到第34周的平均变化总体上升(表示改善)。每次访问研究组之间的EQ-VAS分数没有显著改变(图4)。
•
✦
研究讨论
✦
•
这个三期试验表明安罗替尼、贝莫苏拜单抗和化疗的结合可能在ES-SCLC一线治疗中对病人OS和PFS有利。严重不良事件在两个治疗组发生相对频繁,支持性护理或者剂量调整用来解决这些事件。剂量调整是一个最大化治疗效果减少毒性的常用策略。这个研究的局限性是没有免疫化疗对照。
总结
研究意义
ETER701试验满足了预先计划的中期分析的主要终点,确认了用安罗替尼、贝莫苏拜单抗和化疗结合作为一线治疗和化疗相比能够显著提高ES-SCLC病人的OS,PFS和应答率。和化疗相比,安罗替尼和化疗结合能够提高PFS和应答率,但是OS没有显著差异。
参考文献
[1] Cheng, Y., Chen, J., Zhang, W., Xie, C., Hu, Q., Zhou, N., Huang, C., Wei, S., Sun, H., Li, X., et al. (2024). Benmelstobart, anlotinib and chemotherapy in extensive-stage small-cell lung cancer: a randomized phase 3 trial. Nat Med. Advance online publication. https://doi.org/10.1038/s41591-024-03132-1
END
文案 | 林夕
排版 | 林夕
审核 | 林夕
发布|姜笑南
世界生命科学大会

RECRUIT
关注我们,获取生命科学
学界前沿|促进更多的学术交流与合作
业界前沿|促进更快的产品创新与应用
政策前沿|促进更好的治理实践与发展
