

大蒜作为烹饪的常客,其健康益处早已深入人心。然而,你知道吗,大蒜中的纳米级成分正悄然成为癌症治疗的新希望。最近的研究发现,通过口服大蒜提取的纳米颗粒(GNPs),可以显著激活体内的γδT细胞。这不仅为我们带来了治疗癌症的新思路,也让大蒜这种古老的食材焕发出了新的光彩。

INTRODUCTION
•
✦
研究介绍
✦
•
研究背景
Background
T细胞,作为免疫系统的重要成员,分为αβT细胞和γδT细胞两大类。αβT细胞主要负责识别和攻击外来抗原,而γδT细胞则因其独特的受体结构和不受主要组织相容性复合体限制的特性,在抗癌免疫中展现出巨大的潜力。近年来,基于γδT细胞的免疫疗法逐渐成为癌症治疗的研究热点。然而,传统的过继细胞治疗策略不仅成本高昂、耗时长,还面临扩增γδT细胞的技术挑战。因此,寻找一种能够在体内直接激活和扩增γδT细胞的方法显得尤为重要。
大蒜,这一常见的食材,因其富含的生物活性成分而备受关注。研究表明,大蒜提取物具有免疫调节作用,但传统的补充方式效果有限。而在这项研究中发现大蒜纳米颗粒(GNPs)能够更有效地激活肠道中的γδT细胞,为癌症治疗开辟了新的途径。
基于以上背景,苏州大学汪超、刘庄等人等人在Nature Nanotechnology上发表了题为Oral administration of garlic-derived nanoparticles improves cancer immunotherapy by inducing intestinal IFNγ-producing γδ T cells 的文章。
METHODS
•
✦
研究方法
✦
•
一、GNPs的制备与表征
1.使用两步差分离心法从大蒜中提取GNPs,并通过电镜成像和蛋白质组学分析对其形态和成分进行表征。
2.评估GNPs的稳定性和生物相容性,包括冻干、复水后的粒径变化及形态保持。
二、细胞实验
1.在体外实验中,使用T细胞(Jurkat )、树突状细胞(DC;DC2.4)、巨噬细胞(RAW264.7)以及不同类型的肿瘤细胞(CT26、4T1和B16)评估GNPs的细胞毒性。
2.通过流式细胞术分析GNPs对T细胞(特别是γδ T细胞)的免疫刺激作用,并与大蒜衍生的微粒(GMPs)和裂解性GNPs进行比较。
三、机制研究
1.使用共聚焦成像技术确定GNPs在γδ T细胞上的定位。
2.通过KEGG通路分析,探索GNPs激活γδ T细胞的信号通路。
3.利用β-葡聚糖阻断实验,验证C型凝集素受体信号通路在GNPs激活γδ T细胞中的作用。
四、体内实验
1.给C57BL/6小鼠口服GNPs,并通过DiD标记追踪GNPs在体内的生物分布。
2.评估GNPs对小鼠肠道γδ T细胞增殖、活化的影响,以及这些细胞向肿瘤部位的迁移。
3.研究GNPs处理对肿瘤免疫微环境的影响,并评估其与抗PD-L1协同作用的效果。
RESULTS
•
✦
研究结果
✦
•
通过口服GNPs,成功地在小鼠模型中实现了γδT细胞的内源性扩增和活化。具体而言,GNPs显著促进了肠道内γδT细胞的增殖和活化,导致IFNγ的大量产生。同时,经GNP处理的小鼠肠道γδT细胞中趋化因子CXCR3水平升高,促使这些细胞从肠道迁移到肿瘤环境中。γδT细胞和IFNγ的迁移不仅重塑了肿瘤免疫微环境,还与抗PD-L1协同作用,诱导了强大的抗肿瘤免疫。
进一步的研究表明,GNPs通过直接和间接途径激活γδT细胞。一方面,GNPs定位于γδT细胞表面,通过C型凝集素受体信号通路直接激活γδT细胞;另一方面,GNPs还促进了骨髓衍生树突状细胞(BMDCs)等免疫细胞产生细胞因子(如IL-12p70、IL-6和IL-23),这些细胞因子进一步激活γδT细胞。此外,我们还发现GNPs对多种免疫细胞(包括DC、巨噬细胞和NKT细胞)具有类似的激活作用,进一步增强了其抗肿瘤效果。

图1.GNPs诱导的肠道产IFNγ的γδT细胞。
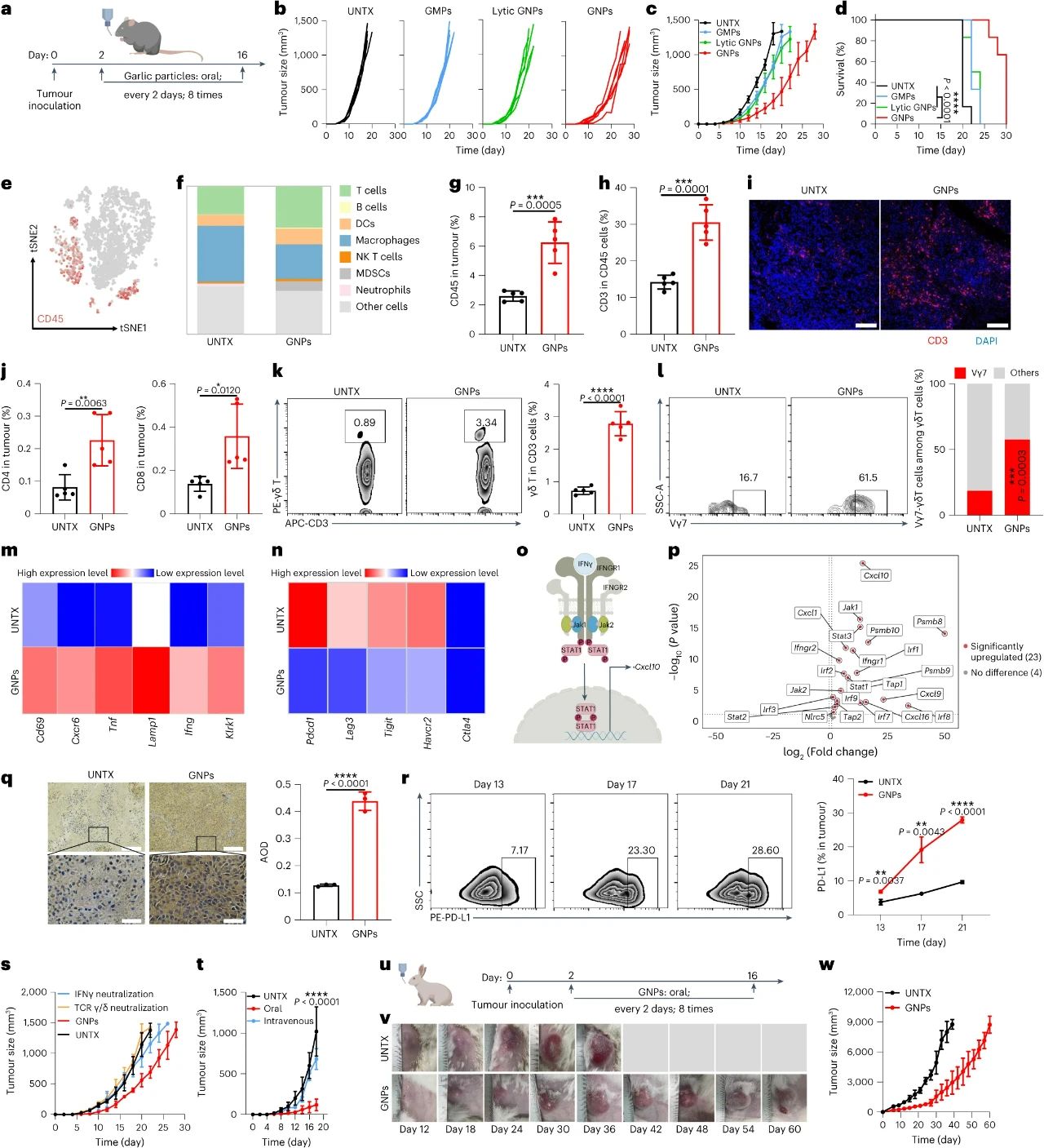
图2.GNPs逆转了远处实体肿瘤的免疫微环境。
HIGHLIGHTS
•
✦
研究亮点
✦
•
1 | 本研究展示了口服GNPs能够显著促进肠道内源性γδ T细胞的增殖和活化,克服了传统过继细胞治疗策略中γδ T细胞扩增、分化等局限性,并揭示了GNPs激活γδ T细胞的机制。 |
2 | 本研究揭示了肠道内γδ T细胞在癌症免疫疗法中的重要作用,以及GNPs在调控肠道-肿瘤相互作用中的潜力,为未来的免疫治疗研究提供了新的方向。 |
参考文献
[1] Xu, J., Yu, Y., Zhang, Y. et al. Oral administration of garlic-derived nanoparticles improves cancer immunotherapy by inducing intestinal IFNγ-producing γδ T cells. Nat. Nanotechnol. (2024). https://doi.org/10.1038/s41565-024-01722-1
END
文案 | 张婷婷
排版 | 张婷婷
审核 | 姜笑南
发布|姜笑南
世界生命科学大会

RECRUIT
关注我们,获取生命科学
学界前沿|促进更多的学术交流与合作
业界前沿|促进更快的产品创新与应用
政策前沿|促进更好的治理实践与发展
我们期待你的加入
RECRUIT
投稿联系:
欢迎加入世界生命科学大会,探索生命医学新未来。
添加微信请备注(单位-专业-姓名)

